Química
Exibindo questões de 501 a 600.
O 1,4-pentanodiol pode sofrer reação de oxidação em - FUVEST 2015
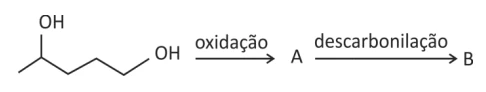
Química - 2015O 1,4-pentanodiol pode sofrer reação de oxidação em condições controladas, com formação de um aldeído A, mantendo o número de átomos de carbono da cadeia. O composto A formado pode, em certas condições, sofrer reação de descarbonilação, isto é, cada uma de suas moléculas perde CO, formando o composto B. O esquema a seguir representa essa sequência de reações:
Uma estudante de Química realizou o seguinte experimento - FUVEST 2015
Química - 2015Uma estudante de Química realizou o seguinte experimento: pesou um tubo de ensaio vazio, colocou nele um pouco de NaHCO3 (s) e pesou novamente. Em seguida, adicionou ao tubo de ensaio excesso de solução aquosa de HCl, o que provocou a reação química representada por
NaHCO3 (s) + HCl (aq) → NaCl (aq) + CO2 (g) + H2O (l)
Após a reação ter-se completado, a estudante aqueceu o sistema cuidadosamente, até que restasse apenas um sólido seco no tubo de ensaio. Deixou o sistema resfriar até a temperatura ambiente e o pesou novamente. A estudante anotou os resultados desse experimento em seu caderno, juntamente com dados obtidos consultando um manual de Química:

A estudante desejava determinar a massa de
I. HCl que não reagiu;
II. NaCl que se formou;
III. CO2 que se formou.
Soluções aquosas de ácido clorídrico, HCl (aq), e de - FUVEST 2015
Química - 2015Soluções aquosas de ácido clorídrico, HCl (aq), e de ácido acético H3CCOOH (aq), ambas de concentração 0,10 mol/L, apresentam valores de pH iguais a 1,0 e 2,9, respectivamente.
Em experimentos separados, volumes iguais de cada uma dessas soluções foram titulados com uma solução aquosa de hidróxido de sódio, NaOH (aq), de concentração adequada. Nessas titulações, a solução de NaOH foi adicionada lentamente ao recipiente contendo a solução ácida, até reação completa. Sejam V1 o volume da solução de NaOH para reação completa com a solução de HCl e V2 o volume da solução de NaOH para reação completa com a solução de H3CCOOH. A relação entre V1 e V2 é
Parte do solo da bacia amazônica é naturalmente pobre em - FUVEST 2015
Química - 2015Parte do solo da bacia amazônica é naturalmente pobre em nutrientes e, consequentemente, pouco apropriada para a agricultura comercial. Por outro lado, em certas porções desse território, são encontradas extensões de terra rica em carvão e nutrientes (sob à forma de compostos de fósforo e cálcio), os quais não resultaram da decomposição microbiana da vegetação. Esse tipo de solo é popularmente chamado de “terra preta”.
Em 2014, na Alemanha, um elemento pesado foi confirmado - FATEC 2015
Química - 2015Em 2014, na Alemanha, um elemento pesado foi confirmado por experimentos com um colisor de partículas e ocupará sua justa posição como Elemento 117 na Tabela Periódica.
Bombardeando amostras de berquélio radioativo com átomos de cálcio, pesquisadores criaram átomos com 117 prótons, originando um elemento químico, aproximadamente, 42% mais pesado que o chumbo e com meia-vida relativamente longa.
Os físicos apelidaram, temporariamente, o novo integrante da Tabela Periódica como “ununséptio” (Uus), alusão direta ao numeral 117, que é a soma dos 20 prótons do cálcio com os 97 do berquélio.
A ardência provocada pela pimenta dedo-de-moça é - FUVEST 2015
Química - 2015A ardência provocada pela pimenta dedo-de-moça é resultado da interação da substância capsaicina com receptores localizados na língua, desencadeando impulsos nervosos que se propagam até o cérebro, o qual interpreta esses impulsos na forma de sensação de ardência. Esse tipo de pimenta tem, entre outros efeitos, o de estimular a sudorese no organismo humano.
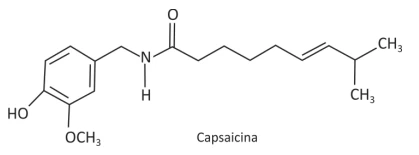
Considere as seguintes afirmações:
I. Nas sinapses, a propagação dos impulsos nervosos, desencadeados pelo consumo dessa pimenta, se dá pela ação de neurotransmissores.
II. Ao consumir essa pimenta, uma pessoa pode sentir mais calor pois, para evaporar, o suor libera calor para o corpo.
III. A hidrólise ácida da ligação amídica da capsaicina produz um aminoácido que é transportado até o cérebro, provocando a sensação de ardência.
A metanfetamina, N-metil-1-fenilpropano-2-amina, fórmula - FATEC 2015
Química - 2015A história do seriado Breaking Bad gira em torno de um professor de Química do ensino médio, com uma esposa grávida e um filho adolescente que sofre de paralisia cerebral. Quando é diagnosticado com câncer, ele abraça uma vida de crimes, produzindo e vendendo metanfetaminas.
O uso de drogas pode desestabilizar totalmente a vida de uma pessoa, gerando consequências devastadoras e permanentes. Muitas vezes, toda a família é afetada.
As metanfetaminas são substâncias relacionadas quimicamente com as anfetaminas e são um potente estimulante que afeta o sistema nervoso central.
(http://tinyurl.com/pffwfe6l. Acessoem: 13.06.2014. Adaptado)
A metanfetamina, N-metil-1-fenilpropano-2-amina, fórmula C10H15N , apresenta os isômeros representados pelas fórmulas estruturais:
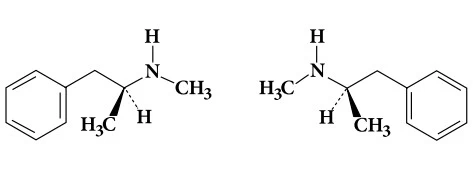
Considere os elementos químicos e seus respectivos - FATEC 2015
Química - 2015A história do seriado Breaking Bad gira em torno de um professor de Química do ensino médio, com uma esposa grávida e um filho adolescente que sofre de paralisia cerebral. Quando é diagnosticado com câncer, ele abraça uma vida de crimes, produzindo e vendendo metanfetaminas.
O uso de drogas pode desestabilizar totalmente a vida de uma pessoa, gerando consequências devastadoras e permanentes. Muitas vezes, toda a família é afetada.
As metanfetaminas são substâncias relacionadas quimicamente com as anfetaminas e são um potente estimulante que afeta o sistema nervoso central.
(http://tinyurl.com/pffwfe6l. Acesso em: 13.06.2014. Adaptado)
Considere os elementos químicos e seus respectivos números atômicos, representados na figura.

O uso de flúor é eficaz no combate à cárie dentária. Por - FATEC 2015
Química - 2015O uso de flúor é eficaz no combate à cárie dentária. Por isso, foram estabelecidos protocolos de utilização do flúor na área de saúde bucal como a adição de flúor na água de abastecimento público e em pastas dentais. A escovação dental é considerada um dos métodos mais eficazes na prevenção da cárie, ao aliar a remoção da placa à exposição constante ao flúor.
Todavia, a exposição excessiva pode causar alguns malefícios à saúde. Para isso, foram estabelecidos níveis seguros de consumo do flúor, quando este oferece o máximo benefício sem risco à saúde. As pastas de dente apresentam uma concentração de flúor que varia entre 1 100 e 1 500 ppm.
É importante ressaltar que as pastas de dente com flúor devem ser utilizadas durante a escovação e não ingeridas.
Após identificar a presença de álcool etílico, H3C— CH2— - FATEC 2015
Química - 2015Após identificar a presença de álcool etílico, H3C— CH2— OH, em amostras de leite cru refrigerado usado por uma empresa na produção de leite longa vida e de requeijão, fiscais da superintendência do Ministério da Agricultura, Pecuária e Abastecimento recomendaram que os lotes irregulares dos produtos fossem recolhidos das prateleiras dos supermercados, conforme prevê o Código de Defesa do Consumidor. Segundo o Ministério, a presença de álcool etílico no leite cru refrigerado pode mascarar a adição irregular de água no produto.
A partir das informações contidas no esquema, é correto - UNESP 2015/2
Química - 2015Leia o texto para responder às questões 68 e 69.
A energia liberada pelo Sol é fundamental para a manutenção da vida no planeta Terra. Grande parte da energia produzida pelo Sol decorre do processo de fusão nuclear em que são formados átomos de hélio a partir de isótopos de hidrogênio, conforme representado no esquema:
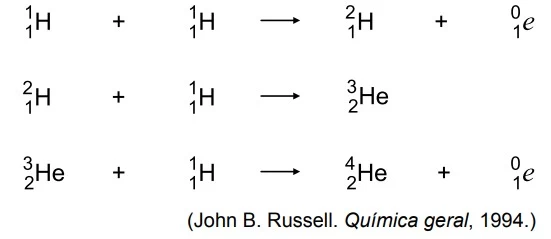
A partir das etapas consecutivas de fusão nuclear - UNESP 2015/2
Química - 2015Leia o texto para responder às questões 68 e 69.
A energia liberada pelo Sol é fundamental para a manutenção da vida no planeta Terra. Grande parte da energia produzida pelo Sol decorre do processo de fusão nuclear em que são formados átomos de hélio a partir de isótopos de hidrogênio, conforme representado no esquema:
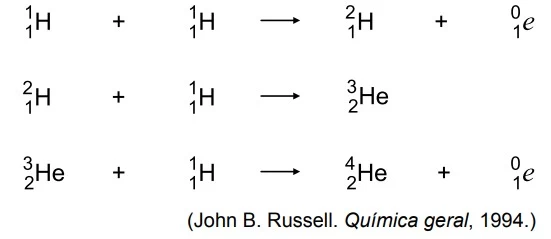
O ácido etanoico, popularmente chamado de ácido - UNESP 2015/2
Química - 2015O ácido etanoico, popularmente chamado de ácido acético, é um ácido fraco e um dos componentes do vinagre, sendo o responsável por seu sabor azedo.
Os protetores solares são formulações que contêm dois - UNESP 2015/2
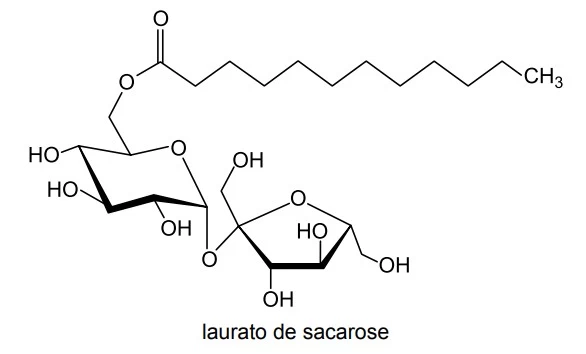
Química - 2015Os protetores solares são formulações que contêm dois componentes básicos: os ingredientes ativos (filtros solares) e os veículos. Dentre os veículos, os cremes e as loções emulsionadas são os mais utilizados, por associarem alta proteção à facilidade de espalhamento sobre a pele. Uma emulsão pode ser obtida a partir da mistura entre óleo e água, por meio da ação de um agente emulsionante. O laurato de sacarose (6-O-laurato de sacarose), por exemplo, é um agente emulsionante utilizado no preparo de emulsões.
Os filtros solares orgânicos absorvem apenas parte da - UNESP 2015/2
Química - 2015Leia o texto para responder às questões de 72 a 74.
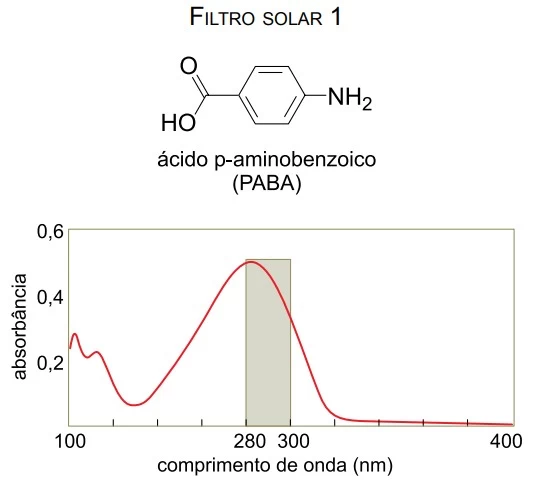
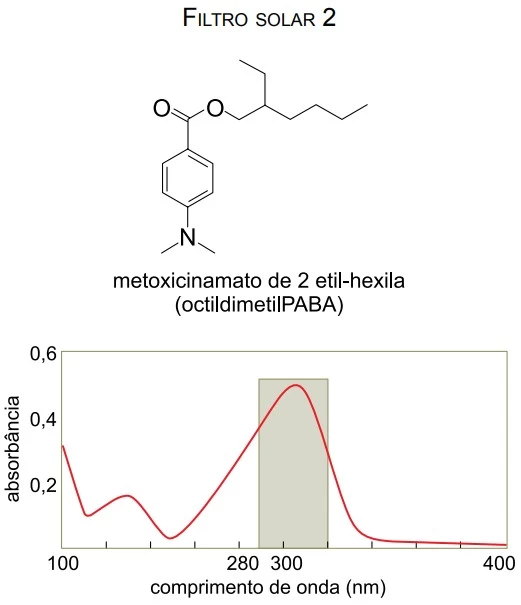
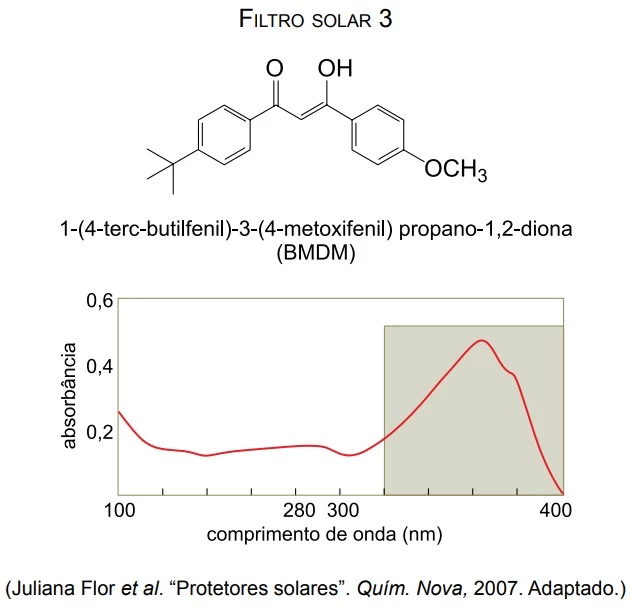
O espectro solar que atinge a superfície terrestre é formado predominantemente por radiações ultravioletas (UV) (100 – 400 nm), radiações visíveis (400 – 800 nm) e radiações infravermelhas (acima de 800 nm). A faixa da radiação UV se divide em três regiões: UVA (320 a 400 nm), UVB (280 a 320 nm) e UVC (100 a 280 nm). Ao interagir com a pele humana, a radiação UV pode provocar reações fotoquímicas, que estimulam a produção de melanina, cuja manifestação é visível sob a forma de bronzeamento da pele, ou podem levar à produção de simples inflamações até graves queimaduras.
Um filtro solar eficiente deve reduzir o acúmulo de lesões induzidas pela radiação UV por meio da absorção das radiações solares, prevenindo assim uma possível queimadura. São apresentados a seguir as fórmulas estruturais, os nomes e os espectros de absorção de três filtros solares orgânicos.
Prazeres, benefícios, malefícios, lucros cercam o mundo - UNICAMP 2015
Química - 2015Prazeres, benefícios, malefícios, lucros cercam o mundo dos refrigerantes. Recentemente, um grande fabricante nacional anunciou que havia reduzido em 13 mil toneladas o uso do açúcar na fabricação de seus refrigerantes, mas não informou em quanto tempo isso ocorreu.
A energia da radiação solar aumenta com a redução de - UNESP 2015/2
Química - 2015Leia o texto para responder às questões de 72 a 74.
O espectro solar que atinge a superfície terrestre é formado predominantemente por radiações ultravioletas (UV) (100 – 400 nm), radiações visíveis (400 – 800 nm) e radiações infravermelhas (acima de 800 nm). A faixa da radiação UV se divide em três regiões: UVA (320 a 400 nm), UVB (280 a 320 nm) e UVC (100 a 280 nm). Ao interagir com a pele humana, a radiação UV pode provocar reações fotoquímicas, que estimulam a produção de melanina, cuja manifestação é visível sob a forma de bronzeamento da pele, ou podem levar à produção de simples inflamações até graves queimaduras.
Um filtro solar eficiente deve reduzir o acúmulo de lesões induzidas pela radiação UV por meio da absorção das radiações solares, prevenindo assim uma possível queimadura. São apresentados a seguir as fórmulas estruturais, os nomes e os espectros de absorção de três filtros solares orgânicos.



Os sprays utilizados em partidas de futebol têm - UNICAMP 2015
Química - 2015Os sprays utilizados em partidas de futebol têm formulações bem variadas, mas basicamente contêm água, butano e um surfactante. Quando essa mistura deixa a embalagem, forma-se uma espuma branca que o árbitro utiliza para marcar as posições dos jogadores.
Dentre os três filtros solares orgânicos citados - UNESP 2015/2
Química - 2015Leia o texto para responder às questões de 72 a 74.
O espectro solar que atinge a superfície terrestre é formado predominantemente por radiações ultravioletas (UV) (100 – 400 nm), radiações visíveis (400 – 800 nm) e radiações infravermelhas (acima de 800 nm). A faixa da radiação UV se divide em três regiões: UVA (320 a 400 nm), UVB (280 a 320 nm) e UVC (100 a 280 nm). Ao interagir com a pele humana, a radiação UV pode provocar reações fotoquímicas, que estimulam a produção de melanina, cuja manifestação é visível sob a forma de bronzeamento da pele, ou podem levar à produção de simples inflamações até graves queimaduras.
Um filtro solar eficiente deve reduzir o acúmulo de lesões induzidas pela radiação UV por meio da absorção das radiações solares, prevenindo assim uma possível queimadura. São apresentados a seguir as fórmulas estruturais, os nomes e os espectros de absorção de três filtros solares orgânicos.



Muito se ouve sobre ações em que se utilizam bombas - UNICAMP 2015
Química - 2015Muito se ouve sobre ações em que se utilizam bombas improvisadas. Nos casos que envolvem caixas eletrônicos, geralmente as bombas são feitas com dinamite (TNT-trinitrotolueno), mas nos atentados terroristas geralmente são utilizados explosivos plásticos, que não liberam odores. Cães farejadores detectam TNT em razão da presença de resíduos de DNT (dinitrotolueno), uma impureza do TNT que tem origem na nitração incompleta do tolueno.
A coloração verde de vegetais se deve à clorofila, uma - UNICAMP 2015
Química - 2015A coloração verde de vegetais se deve à clorofila, uma substância formada por uma base nitrogenada ligada ao íon magnésio, que atua como um ácido de Lewis. Essa coloração não se modifica quando o vegetal está em contato com água fria, mas pode se modificar no cozimento do vegetal. O que leva à mudança de cor é a troca dos íons magnésio por íons hidrogênio, sendo que a molécula da clorofila permanece eletricamente neutra após a troca.
Uma proposta para obter energia limpa é a utilização de - UNICAMP 2015
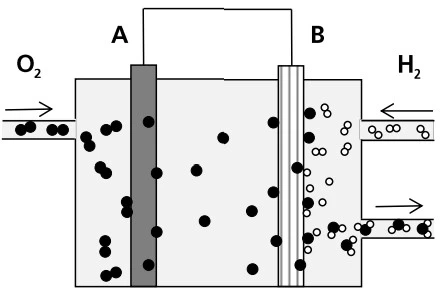
Química - 2015Uma proposta para obter energia limpa é a utilização de dispositivos eletroquímicos que não gerem produtos poluentes, e que utilizem materiais disponíveis em grande quantidade ou renováveis. O esquema abaixo mostra, parcialmente, um dispositivo que pode ser utilizado com essa finalidade.
O hidrogeno carbonato de sódio apresenta muitas - UNICAMP 2015
Química - 2015O hidrogeno carbonato de sódio apresenta muitas aplicações no dia a dia. Todas as aplicações indicadas nas alternativas abaixo são possíveis e as equações químicas apresentadas estão corretamente balanceadas, porém somente em uma alternativa a equação química é coerente com a aplicação.
Hot pack e cold pack são dispositivos que permitem - UNICAMP 2015
Química - 2015Hot pack e cold pack são dispositivos que permitem, respectivamente, aquecer ou resfriar objetos rapidamente e nas mais diversas situações. Esses dispositivos geralmente contêm substâncias que sofrem algum processo quando eles são acionados. Dois processos bastante utilizados nesses dispositivos e suas respectivas energias estão esquematizados nas equações 1 e 2 apresentadas a seguir.

Um importante fator natural que contribui para a - UNICAMP 2015
Química - 2015Um importante fator natural que contribui para a formação de óxidos de nitrogênio na atmosfera são os relâmpagos. Considere um espaço determinado da atmosfera em que haja 20% em massa de oxigênio e 80% de nitrogênio, e que numa tempestade haja apenas formação de dióxido de nitrogênio.
Um artigo científico recente relata um processo de - UNICAMP 2015
Química - 2015Um artigo científico recente relata um processo de produção de gás hidrogênio e dióxido de carbono a partir de metanol e água. Uma vantagem dessa descoberta é que o hidrogênio poderia assim ser gerado em um carro e ali consumido na queima com oxigênio. Dois possíveis processos de uso do metanol como combustível num carro – combustão direta ou geração e gueima do hidrogênio – podem ser equacionados conforme o esquema abaixo:

Quando uma tempestade de poeira atingiu o mar da - UNICAMP 2015
Química - 2015Quando uma tempestade de poeira atingiu o mar da Austrália em 2009, observou-se que a população de fitoplancton aumentou muito. Esse evento serviu de base para um experimento em que a ureia foi utilizada para fertilizar o mar, com o intuito de formar fitoplancton e capturar o CO2 atmosférico. De acordo com a literatura científica, a composição elementar do fitoplancton pode ser representada por C106N16P.
Açaí, castanha-de-caju, castanha-do-brasil e cupuaçu são - FAMERP 2015
Química - 2015Açaí, castanha-de-caju, castanha-do-brasil e cupuaçu são produtos nativos da América do Sul, cada vez mais exportados para Europa. A tabela apresenta um dos constituintes minerais de cada um desses produtos.

O gás carbônico é um dos produtos da reação de - FAMERP 2015
Química - 2015O gás carbônico é um dos produtos da reação de bicarbonato de sódio com solução de ácido clorídrico. Por sua ação antiácida, o bicarbonato de sódio está presente na formulação de alguns medicamentos para alívio de acidez estomacal. A reação descrita é representada na equação:
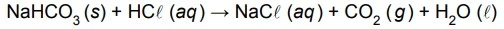
O problema de escassez de água em São Paulo é um tema - FAMERP 2015
Química - 2015O problema de escassez de água em São Paulo é um tema polêmico em discussão que envolve governo e especialistas. O “volume morto”, que passou a ser utilizado em maio de 2014, é um reservatório com 400 milhões de metros cúbicos de água situado abaixo das comportas das represas do Sistema Cantareira.

Uma das substâncias da tabela é muito utilizada como - FAMERP 2015
Química - 2015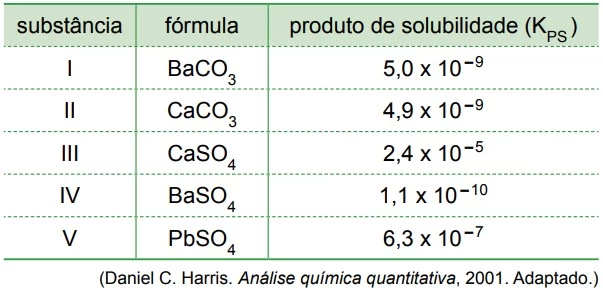
Uma das substâncias da tabela é muito utilizada como meio de contraste em exames radiológicos, pois funciona como um marcador tecidual que permite verificar a integridade da mucosa de todo o trato gastrointestinal, delineando cada segmento. Uma característica necessária ao meio de contraste é que seja o mais insolúvel possível, para evitar que seja absorvido pelos tecidos, tornando-o um marcador seguro, que não será metabolizado no organismo e, portanto, excretado na sua forma intacta.
Uma solução saturada de carbonato de cálcio tem - FAMERP 2015
Química - 2015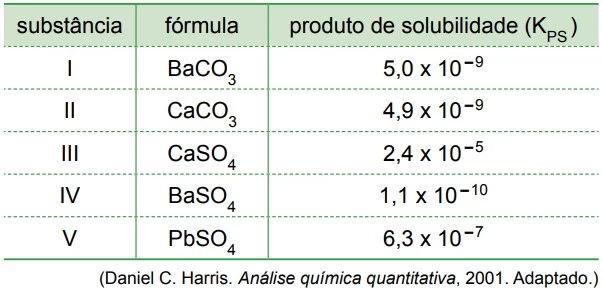
Para realização de certa atividade experimental, os - FAMERP 2015
Química - 2015Para realização de certa atividade experimental, os alunos de uma turma foram organizados em cinco grupos. Cada grupo recebeu uma amostra de um metal que deveria ser identificado e, por isso, os grupos deveriam calcular sua densidade a partir dos valores de massa, determinados em uma balança, e de volume, determinados por meio do deslocamento do volume de água contida em uma proveta.
As cinco amostras recebidas pelos grupos apresentavam-se com as superfícies polidas e suas características são indicadas na tabela.
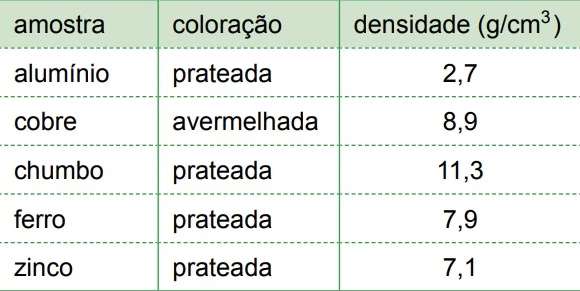
Após constatar que os grupos identificaram corretamente os metais, o professor fez as seguintes observações:
• O metal do grupo 1 tinha coloração avermelhada.
• O metal do grupo 2 tinha menor densidade dentre os metais do experimento.
• O metal do grupo 3 tinha massa = 39,5 g e a proveta utilizada por esse grupo tinha volume de 25 mL com água e de 30 mL com água mais amostra.
• O metal do grupo 4 tinha maior densidade que o do grupo 5.
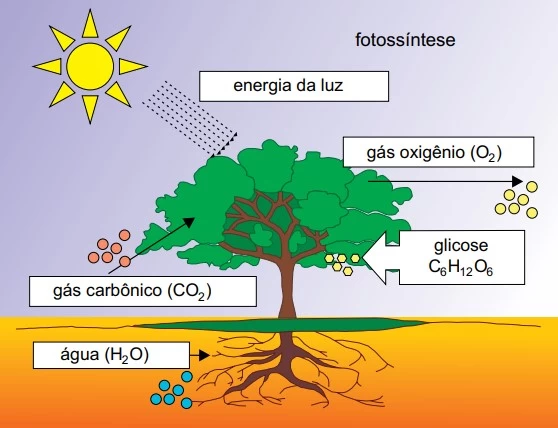
Analise o esquema, que representa o processo de - FAMERP 2015
Química - 2015Analise o esquema, que representa o processo de fotossíntese.
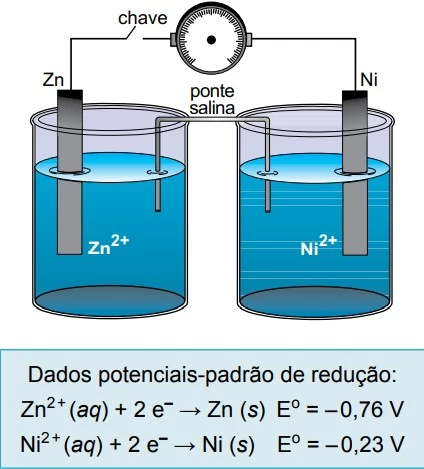
A figura representa o esquema de uma pilha formada com - FAMERP 2015
Química - 2015A figura representa o esquema de uma pilha formada com placas de níquel e zinco mergulhadas em soluções contendo seus respectivos íons.
O que tem futebol a ver com química? Tudo, se o assunto - FAMERP 2015
Química - 2015O que tem futebol a ver com química? Tudo, se o assunto for a bola. Com 12 pentágonos e 20 hexágonos, ela tem a mesma estrutura de uma forma elementar do carbono, chamada de fulereno, cuja descoberta valeu o Nobel de Química de 1996. Na natureza, a molécula é encontrada no espaço interestelar e, em pequenas concentrações, na fumaça do cigarro. Em laboratório, pode ser obtida pela irradiação de uma superfície de grafite com laser. Um fulereno, representado quimicamente como C60 , tem 60 átomos de carbono, assim como a bola tem 60 vértices.
(www.jornaldaciencia.org.br. Adaptado.)
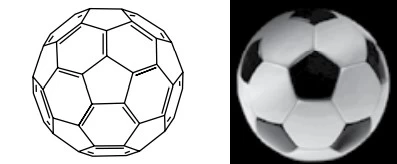
No texto são citados dois __________ do elemento carbono. No C60, cada átomo de carbono faz ___________ ligações sigma.
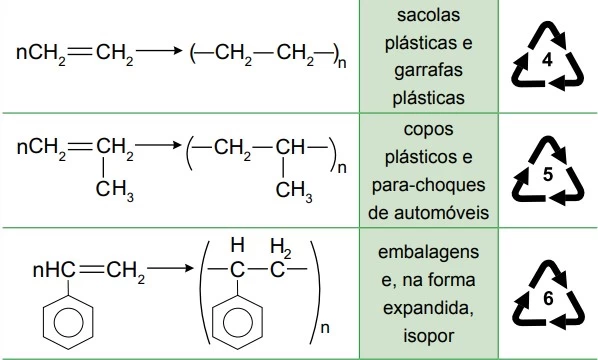
A tabela apresenta as reações de polimerização para - FAMERP 2015
Química - 2015A tabela apresenta as reações de polimerização para obtenção de três importantes polímeros, seus principais usos e seus símbolos de reciclagem.
Um experimento de laboratório para estudo de misturas foi - FGV 2015
Química - 2015Um experimento de laboratório para estudo de misturas foi realizado em uma aula prática, empregando-se as substâncias da tabela seguinte:

Uma embalagem de sopa instantânea apresenta, entre - FUVEST 2014
Química - 2014Uma embalagem de sopa instantânea apresenta, entre outras, as seguintes informações: “Ingredientes: tomate, sal, amido, óleo vegetal, emulsificante, conservante, flavorizante, corante, antioxidante”. Ao se misturar o conteúdo da embalagem com água quente, poderia ocorrer a separação dos componentes X e Y da mistura, formando duas fases, caso o ingrediente Z não estivesse presente.
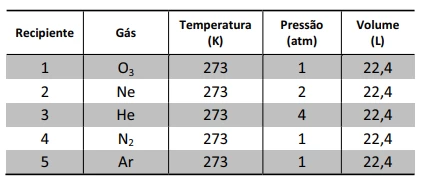
A tabela abaixo apresenta informações sobre cinco gases - FUVEST 2014
Química - 2014A tabela abaixo apresenta informações sobre cinco gases contidos em recipientes separados e selados.
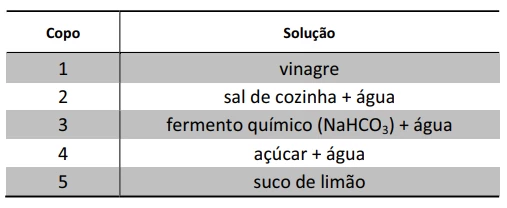
Uma jovem estudante quis demonstrar para sua mãe o que - FUVEST 2014
Química - 2014Uma jovem estudante quis demonstrar para sua mãe o que é uma reação química. Para tanto, preparou, em cinco copos, as seguintes soluções:
Alguns historiadores da Ciência atribuem ao filósofo - VUNESP 2014
Química - 2014Alguns historiadores da Ciência atribuem ao filósofo pré-socrático Empédocles a Teoria dos Quatro Elementos. Segundo essa teoria, a constituição de tudo o que existe no mundo e sua transformação se dariam a partir de quatro elementos básicos: fogo, ar, água e terra. Hoje, a química tem outra definição para elemento: o conjunto de átomos que possuem o mesmo número atômico.
Em um laboratório químico, um estudante encontrou quatro - FUVEST 2014
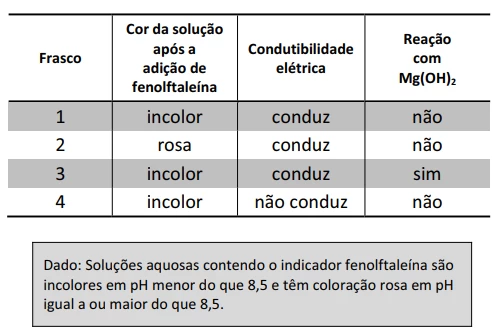
Química - 2014Em um laboratório químico, um estudante encontrou quatro frascos (1, 2, 3 e 4) contendo soluções aquosas incolores de sacarose, KCl, HCl e NaOH, não necessariamente nessa ordem. Para identificar essas soluções, fez alguns experimentos simples, cujos resultados são apresentados na tabela a seguir:
Leia o texto para responder à questão. No ano de 2014, - VUNESP 2014
Química - 2014Leia o texto para responder à questão.
No ano de 2014, o Estado de São Paulo vive uma das maiores crises hídricas de sua história. A fim de elevar o nível de água de seus reservatórios, a Companhia de Saneamento Básico do Estado de São Paulo (Sabesp) contratou a empresa ModClima para promover a indução de chuvas artificiais. A técnica de indução adotada, chamada de bombardeamento de nuvens ou semeadura ou, ainda, nucleação artificial, consiste no lançamento em nuvens de substâncias aglutinadoras que ajudam a formar gotas de água.
Uma usina de reciclagem de plástico recebeu um lote de - FUVEST 2014
Química - 2014Uma usina de reciclagem de plástico recebeu um lote de raspas de 2 tipos de plásticos, um deles com densidade 1,10 kg/L e outro com densidade 1,14 kg/L. Para efetuar a separação dos dois tipos de plásticos, foi necessário preparar 1000 L de uma solução de densidade apropriada, misturando-se volumes adequados de água (densidade = 1,00 kg/L) e de uma solução aquosa de NaCl, disponível no almoxarifado da usina, de densidade 1,25 kg/L. Esses volumes, em litros, podem ser, respectivamente,
Além do iodeto de prata, outras substâncias podem ser - VUNESP 2014
Química - 2014Leia o texto para responder à questão.
No ano de 2014, o Estado de São Paulo vive uma das maiores crises hídricas de sua história. A fim de elevar o nível de água de seus reservatórios, a Companhia de Saneamento Básico do Estado de São Paulo (Sabesp) contratou a empresa ModClima para promover a indução de chuvas artificiais. A técnica de indução adotada, chamada de bombardeamento de nuvens ou semeadura ou, ainda, nucleação artificial, consiste no lançamento em nuvens de substâncias aglutinadoras que ajudam a formar gotas de água.
(http://exame.abril.com.br. Adaptado.)
A aparelhagem esquematizada na figura abaixo pode ser - FUVEST 2014
Química - 2014A aparelhagem esquematizada na figura abaixo pode ser utilizada para identificar gases ou vapores produzidos em transformações químicas. No frasco 1, cristais azuis de CoCl2 anidro adquirem coloração rosa em contato com vapor d’água. No frasco 2, a solução aquosa saturada de Ca(OH)2 turva-se em contato com CO2 (g).
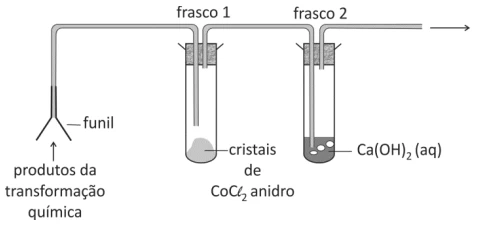
Utilizando essa aparelhagem em três experimentos distintos, um estudante de Química investigou os produtos obtidos em três diferentes processos:
I. aquecimento de CaCO3 puro;
II. combustão de uma vela;
III. reação de raspas de Mg (s) com HCl (aq).
Para a produção de chuva artificial, um avião adaptado - VUNESP 2014
Química - 2014Leia o texto para responder à questão.
No ano de 2014, o Estado de São Paulo vive uma das maiores crises hídricas de sua história. A fim de elevar o nível de água de seus reservatórios, a Companhia de Saneamento Básico do Estado de São Paulo (Sabesp) contratou a empresa ModClima para promover a indução de chuvas artificiais. A técnica de indução adotada, chamada de bombardeamento de nuvens ou semeadura ou, ainda, nucleação artificial, consiste no lançamento em nuvens de substâncias aglutinadoras que ajudam a formar gotas de água.
(http://exame.abril.com.br. Adaptado.)
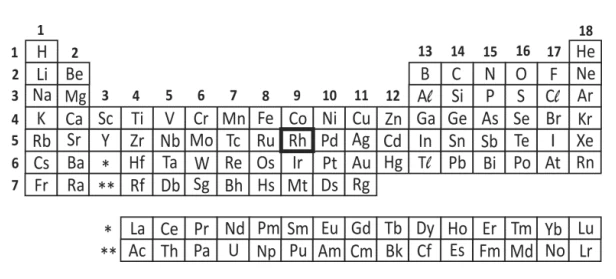
Observe a posição do elemento químico ródio (Rh) na - FUVEST 2014
Química - 2014Observe a posição do elemento químico ródio (Rh) na tabela periódica.
Leia o texto para responder à questão. Uma medida - VUNESP 2014
Química - 2014Leia o texto para responder à questão.
Uma medida adotada pelo governo do estado para amenizar a crise hídrica que afeta a cidade de São Paulo envolve a utilização do chamado “volume morto” dos reservatórios do Sistema Cantareira. Em artigo publicado pelo jornal O Estado de S.Paulo, três especialistas alertam sobre os riscos trazidos por esse procedimento que pode trazer à tona poluentes depositados no fundo das represas, onde se concentram contaminantes que não são tratados por sistemas convencionais. Entre os poluentes citados que contaminam os mananciais há compostos inorgânicos, orgânicos altamente reativos com os sistemas biológicos, microbiológicos e vírus. Segundo as pesquisadoras, “quanto mais baixo o nível dos reservatórios, maior é a concentração de poluentes, recomendando maiores cuidados”.
(http://sao-paulo.estadao.com.br. Adaptado.)
De modo geral, em sistemas aquáticos a decomposição de matéria orgânica de origem biológica, na presença de oxigênio, se dá por meio de um processo chamado degradação aeróbica. As equações representam reações genéricas envolvidas na degradação aeróbica, em que “MO” = matéria orgânica contendo nitrogênio e enxofre.
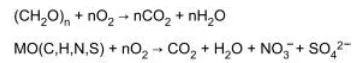
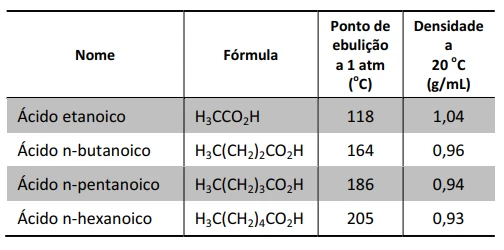
A tabela a seguir contém dados sobre alguns ácidos - FUVEST 2014
Química - 2014A tabela a seguir contém dados sobre alguns ácidos carboxílicos.
Estudos ambientais revelaram que o ferro é um dos metais - FGV 2015
Química - 2014Estudos ambientais revelaram que o ferro é um dos metais presentes em maior quantidade na atmosfera, apresentando-se na forma do íon de ferro 3+ hidratado, [Fe(H2O)6]3+. O íon de ferro na atmosfera se hidrolisa de acordo com a equação
[Fe(H2 O)6 ] 3+ ↔ [Fe(H2 O)5 OH]2+ + H+
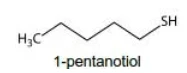
A degradação anaeróbica de matéria orgânica contendo - VUNESP 2014
Química - 2014A degradação anaeróbica de matéria orgânica contendo enxofre pode levar à formação de substâncias com odores altamente desagradáveis. Dentre essas substâncias estão o gás sulfídrico (H2 S) e as mercaptanas, como a pentamercaptana (1-pentanotiol).
O rótulo de uma lata de desodorante em aerosol apresenta - FUVEST 2014
Química - 2014O rótulo de uma lata de desodorante em aerosol apresenta, entre outras, as seguintes informações: “Propelente: gás butano. Mantenha longe do fogo”. A principal razão dessa advertência é:
Leia o texto para responder à questão. Água coletada - VUNESP 2014
Química - 2014Leia o texto para responder à questão.
Água coletada em Fukushima em 2013 revela radioatividade recorde
A empresa responsável pela operação da usina nuclear de Fukushima, Tokyo Electric Power (Tepco), informou que as amostras de água coletadas na central em julho de 2013 continham um nível recorde de radioatividade, cinco vezes maior que o detectado originalmente. A Tepco explicou que uma nova medição revelou que o líquido, coletado de um poço de observação entre os reatores 1 e 2 da fábrica, continha nível recorde do isótopo radioativo estrôncio-90.
(www.folha.uol.com.br. Adaptado.)
O isótopo radioativo Sr-90 não existe na natureza, sua formação ocorre principalmente em virtude da desintegração do Br-90 resultante do processo de fissão do urânio e do plutônio em reatores nucleares ou em explosões de bombas atômicas. Observe a série radioativa, a partir do Br-90, até a formação do Sr-90:
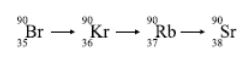
A adição de um soluto à água altera a temperatura de - FUVEST 2014
Química - 2014A adição de um soluto à água altera a temperatura de ebulição desse solvente. Para quantificar essa variação em função da concentração e da natureza do soluto, foram feitos experimentos, cujos resultados são apresentados abaixo. Analisando a tabela, observa-se que a variação de temperatura de ebulição é função da concentração de moléculas ou íons de soluto dispersos na solução.
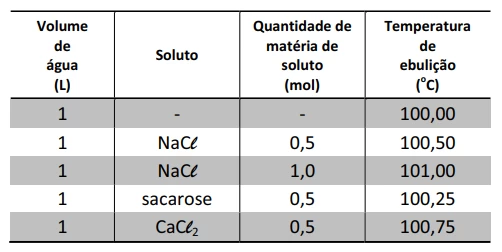
Dois novos experimentos foram realizados, adicionando-se 1 mol de Na2SO4 a 1 Lde água (experimento A) e 1,0 mol de glicose a 0,5 L de água (experimento B). Considere que os resultados desses novos experimentos tenham sido consistentes com os experimentos descritos na tabela.
Estudos recentes parecem indicar que o formato do olho - FUVEST 2014
Química - 2014Estudos recentes parecem indicar que o formato do olho humano e a visão são influenciados pela quantidade da substância X, sintetizada pelo organismo. A produção dessa substância é favorecida pela luz solar, e crianças que fazem poucas atividades ao ar livre tendem a desenvolver dificuldade para enxergar objetos distantes. Essa disfunção ocular é comumente chamada de miopia. Considere a fórmula estrutural da substância X e os diferentes formatos de olho:
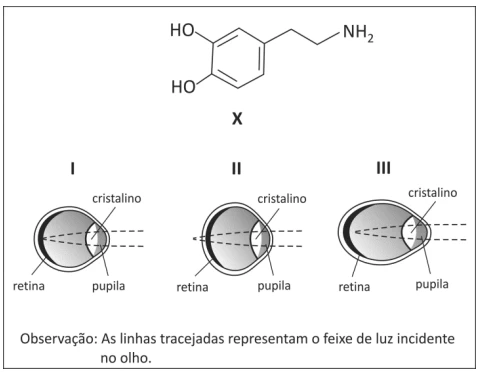
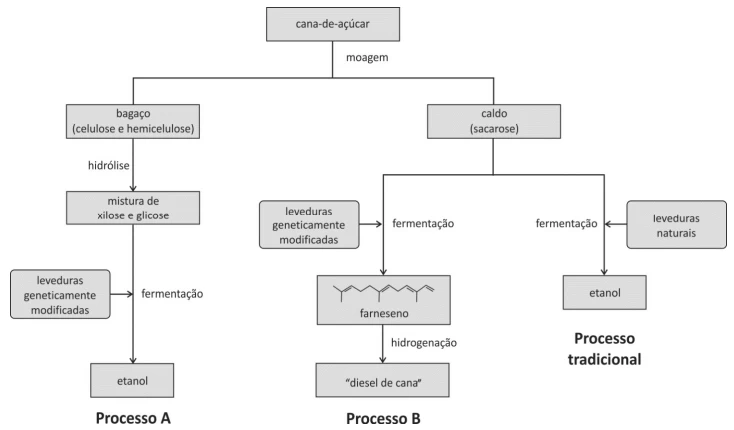
No processo tradicional, o etanol é produzido a partir - FUVEST 2014
Química - 2014No processo tradicional, o etanol é produzido a partir do caldo da cana-de-açúcar por fermentação promovida por leveduras naturais, e o bagaço de cana é desprezado. Atualmente, leveduras geneticamente modificadas podem ser utilizadas em novos processos de fermentação para a produção de biocombustíveis. Por exemplo, no processo A, o bagaço de cana, após hidrólise da celulose e da hemicelulose, também pode ser transformado em etanol. No processo B, o caldo de cana, rico em sacarose, é transformado em farneseno que, após hidrogenação das ligações duplas, se transforma no "diesel de cana". Esses três processos de produção de biocombustíveis podem ser representados por:
Uma nova e promissora classe de materiais supercondutores - FGV 2014
Química - 2014Uma nova e promissora classe de materiais supercondutores tem como base o composto diboreto de zircônio e vanádio. Esse composto é sintetizado a partir de um sal de zircônio (IV).
O conhecimento das propriedades físico-químicas das - FGV 2014
Química - 2014O conhecimento das propriedades físico-químicas das substâncias é muito útil para avaliar condições adequadas para a sua armazenagem e transporte.
Considere os dados das três substâncias seguintes:

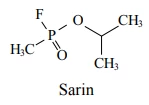
Armas químicas são baseadas na toxicidade de substâncias, - FGV 2014
Química - 2014Armas químicas são baseadas na toxicidade de substâncias, capazes de matar ou causar danos a pessoas e ao meio ambiente. Elas têm sido utilizadas em grandes conflitos e guerras, como o ocorrido em 2013 na Síria, quando a ação do sarin causou a morte de centenas de civis.
(http://pt.wikipedia.org/wiki/Guerra_qu%C3%ADmica e http://pt.wikipedia.org/wiki/Categoria:Armas_qu%C3%ADmicas. Adaptado)
Créditos de carbono são certificações dadas a empresas, - FGV 2014
Química - 2014Créditos de carbono são certificações dadas a empresas, indústrias e países que conseguem reduzir a emissão de gases poluentes na atmosfera. Cada tonelada de CO2 não emitida ou retirada da atmosfera equivale a um crédito de carbono.
No decaimento do amerício-241 a neptúnio-237, há emissão de - FGV 2014
Química - 2014O texto seguinte refere-se à questão
Deverá entrar em funcionamento em 2017, em Iperó, no interior de São Paulo, o Reator Multipropósito Brasileiro (RMB), que será destinado à produção de radioisótopos para radiofármacos e também para produção de fontes radioativas usadas pelo Brasil em larga escala nas áreas industrial e de pesquisas. Um exemplo da aplicação tecnológica de radioisótopos são sensores contendo fonte de amerício-241, obtido como produto de fissão. Ele decai para o radioisótopo neptúnio-237 e emite um feixe de radiação. Fontes de amerício-241 são usadas como indicadores de nível em tanques e fornos mesmo em ambiente de intenso calor, como ocorre no interior dos alto fornos da Companhia Siderúrgica Paulista (COSIPA).
A produção de combustível para os reatores nucleares de fissão envolve o processo de transformação do composto sólido UO2 ao composto gasoso UF6 por meio das etapas:

Considerando o tipo de reator mencionado no texto, - FGV 2014
Química - 2014O texto seguinte refere-se à questão
Deverá entrar em funcionamento em 2017, em Iperó, no interior de São Paulo, o Reator Multipropósito Brasileiro (RMB), que será destinado à produção de radioisótopos para radiofármacos e também para produção de fontes radioativas usadas pelo Brasil em larga escala nas áreas industrial e de pesquisas. Um exemplo da aplicação tecnológica de radioisótopos são sensores contendo fonte de amerício-241, obtido como produto de fissão. Ele decai para o radioisótopo neptúnio-237 e emite um feixe de radiação. Fontes de amerício-241 são usadas como indicadores de nível em tanques e fornos mesmo em ambiente de intenso calor, como ocorre no interior dos alto fornos da Companhia Siderúrgica Paulista (COSIPA).
A produção de combustível para os reatores nucleares de fissão envolve o processo de transformação do composto sólido UO2 ao composto gasoso UF6 por meio das etapas:

Considere os dados da tabela: O valor da entalpia padrão - FGV 2014
Química - 2014O texto seguinte refere-se à questão
Deverá entrar em funcionamento em 2017, em Iperó, no interior de São Paulo, o Reator Multipropósito Brasileiro (RMB), que será destinado à produção de radioisótopos para radiofármacos e também para produção de fontes radioativas usadas pelo Brasil em larga escala nas áreas industrial e de pesquisas. Um exemplo da aplicação tecnológica de radioisótopos são sensores contendo fonte de amerício-241, obtido como produto de fissão. Ele decai para o radioisótopo neptúnio-237 e emite um feixe de radiação. Fontes de amerício-241 são usadas como indicadores de nível em tanques e fornos mesmo em ambiente de intenso calor, como ocorre no interior dos alto fornos da Companhia Siderúrgica Paulista (COSIPA).
A produção de combustível para os reatores nucleares de fissão envolve o processo de transformação do composto sólido UO2 ao composto gasoso UF6 por meio das etapas:

O Brasil é um grande produtor e exportador de suco - FGV 2014
Química - 2014O Brasil é um grande produtor e exportador de suco concentrado de laranja. O suco in natura é obtido a partir de processo de prensagem da fruta que, após a separação de cascas e bagaços, possui 12% em massa de sólidos totais, solúveis e insolúveis. A preparação do suco concentrado é feita por evaporação de água até que se atinja o teor de sólidos totais de 48% em massa
O composto inorgânico alaranjado dicromato de amônio, - FGV 2014
Química - 2014O composto inorgânico alaranjado dicromato de amônio, (NH4)2 Cr2 O7 , quando aquecido sofre decomposição térmica em um processo que libera água na forma de vapor, gás nitrogênio e também forma o óxido de cromo (III). Esse fenômeno ocorre com uma grande expansão de volume e, por isso, é usado em simulações de efeitos de explosões vulcânicas com a denominação de vulcão químico.

A indústria alimentícia emprega várias substâncias químicas - FGV 2014
Química - 2014A indústria alimentícia emprega várias substâncias químicas para conservar os alimentos e garantir que eles se mantenham adequados para consumo após a fabricação, transporte e armazenagem nos pontos de venda. Dois exemplos disso são o nitrato de sódio adicionado nos produtos derivados de carnes e o sorbato de potássio, proveniente do ácido sórbico HC6H7O2 (Ka = 2 x 10–5 a 25°C), usado na fabricação de queijos.
A amônia é um composto muito versátil, pois seu - FGV 2014
Química - 2014A amônia é um composto muito versátil, pois seu comportamento químico possibilita seu emprego em várias reações químicas em diversos mecanismos reacionais, como em
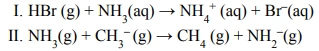
De acordo com o conceito ácido-base de Lewis, em I a amônia é classificada como _________. De acordo com o conceito ácido-base de Brösnted-Lowry, a amônia é classificada em I e II, respectivamente, como_________ e _________.
Para otimizar as condições de um processo industrial que - FGV 2014
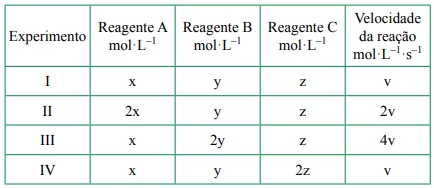
Química - 2014Para otimizar as condições de um processo industrial que depende de uma reação de soluções aquosas de três diferentes reagentes para a formação de um produto, um engenheiro químico realizou um experimento que consistiu em uma série de reações nas mesmas condições de temperatura e agitação. Os resultados são apresentados na tabela:
A fórmula molecular e o total de ligações sigma na molécula - FGV 2014
Química - 2014texto a seguir refere-se à questão
O conhecimento científico tem sido cada vez mais empregado como uma ferramenta na elucidação de crimes. A química tem fornecido muitas contribuições para a criação da ciência forense. Um exemplo disso são as investigações de impressões digitais empregando-se a substância I (figura). Essa substância interage com resíduos de proteína deixados pelo contato das mãos e, na presença de uma fonte de luz adequada, luminesce e revela vestígios imperceptíveis a olho nu.
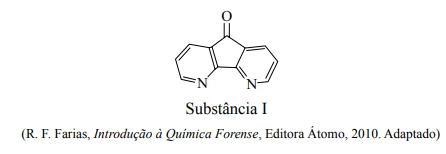
Na estrutura da substância I, observam-se as funções - FGV 2014
Química - 2014texto a seguir refere-se à questão
O conhecimento científico tem sido cada vez mais empregado como uma ferramenta na elucidação de crimes. A química tem fornecido muitas contribuições para a criação da ciência forense. Um exemplo disso são as investigações de impressões digitais empregando-se a substância I (figura). Essa substância interage com resíduos de proteína deixados pelo contato das mãos e, na presença de uma fonte de luz adequada, luminesce e revela vestígios imperceptíveis a olho nu.

De acordo com dados da Agência Internacional de Energia - FGV 2014
Química - 2014De acordo com dados da Agência Internacional de Energia (AIE), aproximadamente 87% de todo o combustível consumido no mundo são de origem fóssil. Essas substâncias são encontradas em diversas regiões do planeta, no estado sólido, líquido e gasoso e são processadas e empregadas de diversas formas.
(www.brasilescola.com/geografia/combustiveis-fosseis.htm. Adaptado)
Por meio de processo de destilação seca, o combustível I dá origem à matéria-prima para a indústria de produção de aço e alumínio.O combustível II é utilizado como combustível veicular, em usos domésticos, na geração de energia elétrica e também como matéria-prima em processos industriais.
O combustível III é obtido por processo de destilação fracionada ou por reação química, e é usado como combustível veicular.
O Brasil inaugurou em 2014 o Projeto Sirius, um acelerador - FGV 2015
Química - 2014O Brasil inaugurou em 2014 o Projeto Sirius, um acelerador de partículas que permitirá o desenvolvimento de pesquisa na área de materiais, física, química e biologia. Seu funcionamento se dará pelo fornecimento de energia a feixes de partículas subatômicas eletricamente carregadas: prótons e elétrons.
(http://www.brasil.gov.br/ciencia-e-tecnologia/2014/02/. Adaptado)
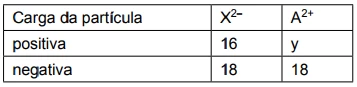
Na tabela, são apresentadas informações das quantidades de algumas partículas subatômicas para os íons X2– e A2+:
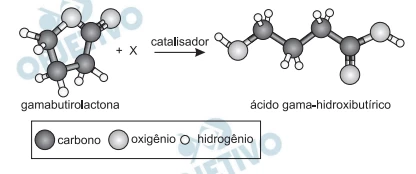
O ácido gama-hidroxibutírico é utilizado no tratamento - FUVEST 2013
Química - 2013O ácido gama-hidroxibutírico é utilizado no tratamento do alcoolismo. Esse ácido pode ser obtido a partir da gamabutirolactona, conforme a representação a seguir:
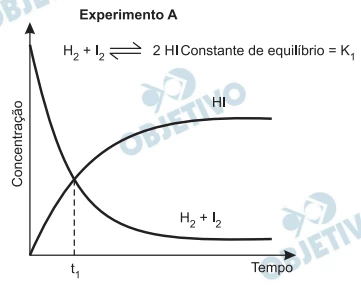
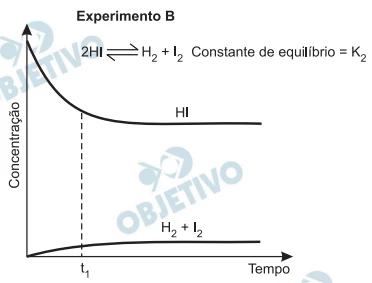
A uma determinada temperatura, as substâncias HI, H2 e - FUVEST 2013
Química - 2013A uma determinada temperatura, as substâncias HI, H2 e I2 estão no estado gasoso. A essa temperatura, o equilíbrio entre as três substâncias foi estudado, em recipientes fechados, partindo-se de uma mistura equimolar de H2 e I2 (experimento A) ou somente de HI (experimento B).
Quando certos metais são colocados em contato com - FUVEST 2013
Química - 2013Quando certos metais são colocados em contato com soluções ácidas, pode haver formação de gás hidrogênio. Abaixo, segue uma tabela elaborada por uma estudante de Química, contendo resultados de experimentos que ela realizou em diferentes condições.
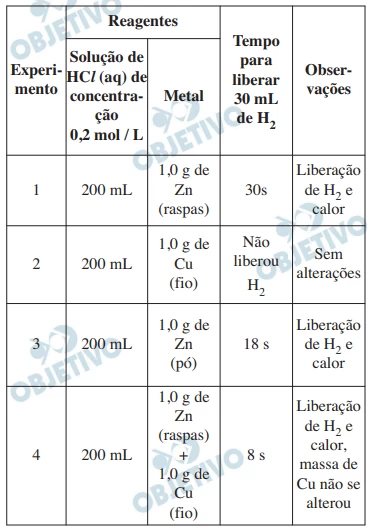
Após realizar esses experimentos, a estudante fez três afirmações:
I. A velocidade da reação de Zn com ácido aumenta na presença de Cu.
II. O aumento na concentração inicial do ácido causa o aumento da velocidade de liberação do gás H2.
III. Os resultados dos experimentos 1 e 3 mostram que, quanto maior o quociente superfície de contato/massa total de amostra de Zn, maior a velocidade de reação.
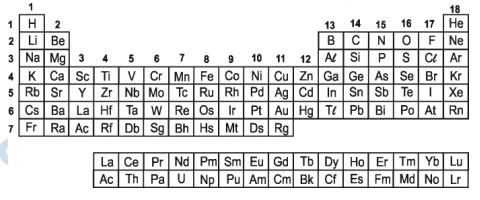
Um aluno estava analisando a Tabela Periódica e - FUVEST 2013
Química - 2013Um aluno estava analisando a Tabela Periódica e encontrou vários conjuntos de três elementos químicos que apresentavam propriedades semelhantes.
O craqueamento catalítico é um processo utilizado na - FUVEST 2013
Química - 2013O craqueamento catalítico é um processo utilizado na indústria petroquímica para converter algumas frações do petróleo que são mais pesadas (isto é, constituídas por compostos de massa molar elevada) em frações mais leves, como a gasolina e o GLP, por exemplo. Nesse processo, algumas ligações químicas nas moléculas de grande massa molecular são rompidas, sendo geradas moléculas menores.
A respeito desse processo, foram feitas as seguintes afirmações:
I. O craqueamento é importante economicamente, pois converte frações mais pesadas de petróleo em compostos de grande demanda.
II. O craqueamento libera grande quantidade de energia, proveniente da ruptura de ligações químicas nas moléculas de grande massa molecular.
III. A presença de catalisador permite que as transformações químicas envolvidas no craqueamento ocorram mais rapidamente.
A porcentagem em massa de sais no sangue é de - FUVEST 2013
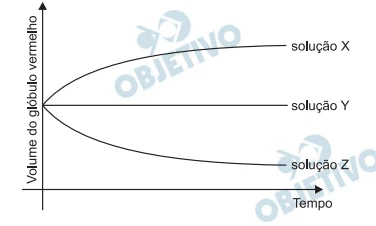
Química - 2013A porcentagem em massa de sais no sangue é de aproximadamente 0,9%. Em um experimento, alguns glóbulos vermelhos de uma amostra de sangue foram coletados e separados em três grupos. Foram preparadas três soluções, identificadas por X, Y e Z, cada qual com uma diferente concentração salina. A cada uma dessas soluções foi adicionado um grupo de glóbulos vermelhos. Para cada solução, acompanhou-se, ao longo do tempo, o volume de um glóbulo vermelho, como mostra o gráfico.
A partir de considerações teóricas, foi feita uma - FUVEST 2013
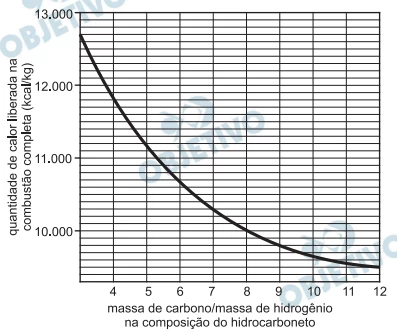
Química - 2013A partir de considerações teóricas, foi feita uma estimativa do poder calorífico (isto é, da quantidade de calor liberada na combustão completa de 1 kg de combustível) de grande número de hidrocarbonetos. Dessa maneira, foi obtido o seguinte gráfico de valores teóricos:
Um funcionário de uma empresa ficou encarregado de - FUVEST 2013
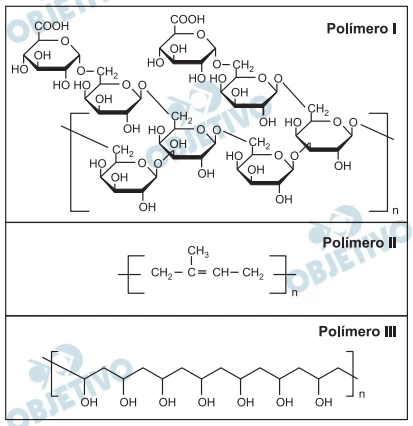
Química - 2013Um funcionário de uma empresa ficou encarregado de remover resíduos de diferentes polímeros que estavam aderidos a diversas peças. Após alguma investigação, o funcionário classificou as peças em três grupos, conforme o polímero aderido a cada uma. As fórmulas estruturais de cada um desses polímeros são as seguintes:
Uma moeda antiga de cobre estava recoberta com uma - FUVEST 2013
Química - 2013Uma moeda antiga de cobre estava recoberta com uma camada de óxido de cobre (II). Para restaurar seu brilho original, a moeda foi aquecida ao mesmo tempo em que se passou sobre ela gás hidrogênio. Nesse processo, formou-se vapor de água e ocorreu a redução completa do cátion metálico.
As massas da moeda, antes e depois do processo descrito, eram, respectivamente, 0,795 g e 0,779 g.
Dados: Massas molares (g/mol)
H = 1,00
O = 16,0
Cu = 63,5
O fitoplâncton consiste em um conjunto de organismos - FUVEST 2013
Química - 2013O fitoplâncton consiste em um conjunto de organismos microscópicos encontrados em certos ambientes aquáticos. O desenvolvimento desses organismos requer luz e CO2, para o processo de fotossíntese, e requer também nutrientes contendo os elementos nitrogênio e fósforo.
Considere a tabela que mostra dados de pH e de concentrações de nitrato e de oxigênio dissolvidos na água, para amostras coletadas durante o dia, em dois diferentes pontos (A e B) e em duas épocas do ano (maio e novembro), na represa Billings, em São Paulo
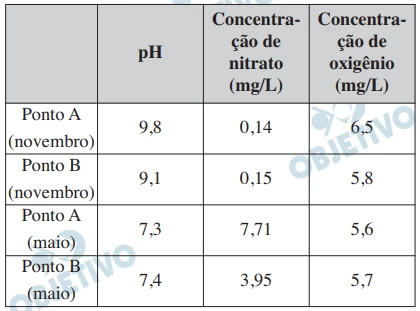
Com base nas informações da tabela e em seus próprios conhecimentos sobre o processo de fotossíntese, um pesquisador registrou três conclusões:
I. Nessas amostras, existe uma forte correlação entre as concentrações de nitrato e de oxigênio dissolvidos na água.
II. As amostras de água coletadas em novembro devem ter menos CO2 dissolvido do que aquelas coletadas em maio.
III. Se as coletas tivessem sido feitas à noite, o pH das quatro amostras de água seria mais baixo do que o observado.
Admite-se que as cenouras sejam originárias da região do - FUVEST 2013
Química - 2013Admite-se que as cenouras sejam originárias da região do atual Afeganistão, tendo sido levadas para outras partes do mundo por viajantes ou invasores. Com base em relatos escritos, pode-se dizer que as cenouras devem ter sido levadas à Europa no século XII e, às Américas, no início do século XVII.
Em escritos anteriores ao século XVI, há referência apenas a cenouras de cor roxa, amarela ou vermelha. É possível que as cenouras de cor laranja sejam originárias dos Países Baixos, e que tenham sido desenvolvidas, inicialmente, à época do Príncipe de Orange (1533-1584). No Brasil, são comuns apenas as cenouras laranja, cuja cor se deve à presença do pigmento betacaroteno, representado a seguir.
Louis Pasteur realizou experimentos pioneiros em - FUVEST 2013
Química - 2013Louis Pasteur realizou experimentos pioneiros em Microbiologia. Para tornar estéril um meio de cultura, o qual poderia estar contaminado com agentes causadores de doenças, Pasteur mergulhava o recipiente que o continha em um banho de água aquecida à ebulição e à qual adicionava cloreto de sódio. Com a adição de cloreto de sódio, a temperatura de ebulição da água do banho, com relação à da água pura, era ______. O aquecimento do meio de cultura provocava _______.
Em um recipiente termicamente isolado e mantido a - FUVEST 2013
Química - 2013Em um recipiente termicamente isolado e mantido a pressão constante, são colocados 138g de etanol líquido. A seguir, o etanol é aquecido e sua temperatura T é medida como função da quantidade de calor Q a ele transferida.
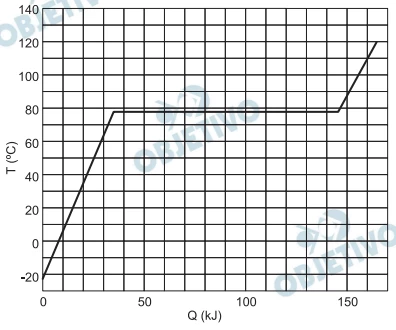
A vanilina, 4-hidroxi-3-metoxibenzaldeído, fórmula C8 - VUNESP 2013
Química - 2013A vanilina, 4-hidroxi-3-metoxibenzaldeído, fórmula C8 H8 O3 , é responsável pelo aroma e sabor de baunilha, muito apreciados no mundo inteiro. É obtida tradicionalmente das vagens, também chamadas de favas, de uma orquídea tropical, a Vanilla planifolia.
A figura mostra um processo de extração da vanilina a partir de vagens de orquídea espalhadas sobre bandejas perfuradas, em tanques de aço, usando etanol (60% v/v) como solvente. Em geral, a extração dura duas semanas.
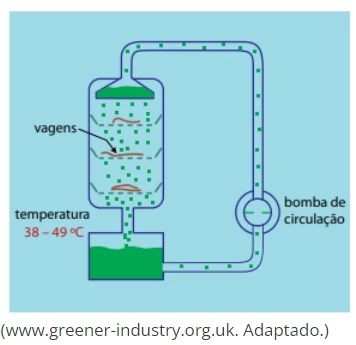
Alimento enriquecido é todo alimento ao qual foi - VUNESP 2013
Química - 2013Alimento enriquecido é todo alimento ao qual foi adicionada uma substância nutriente, com o objetivo de reforçar o seu valor nutritivo. A vitamina C, estrutura representada na figura, é uma das vitaminas utilizadas na suplementação de alimentos.
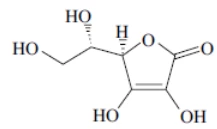
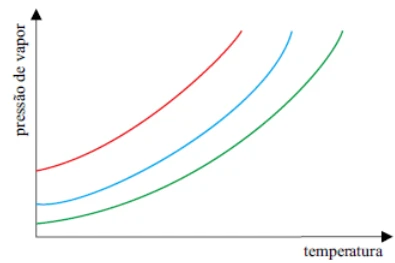
Na figura estão representadas as curvas pressão de vapor - VUNESP 2013
Química - 2013Na figura estão representadas as curvas pressão de vapor x temperatura para três solventes puros: benzeno (curva vermelha), água (curva azul) e ácido acético (curva verde).
Na obra O poço do Visconde, de Monteiro Lobato, há o - FUVEST 2012
Química - 2012Na obra O poço do Visconde, de Monteiro Lobato, há o seguinte diálogo entre o Visconde de Sabugosa e a boneca Emília:
– Senhora Emília, explique-me o que é hidrocarboneto. A atrapalhadeira não se atrapalhou e respondeu:
– São misturinhas de uma coisa chamada hidrogênio com outra coisa chamada carbono. Os carocinhos de um se ligam aos carocinhos de outro.
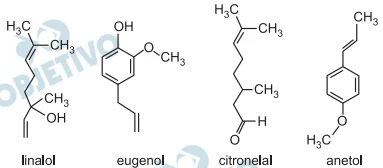
As fórmulas estruturais de alguns componentes de óleos - FUVEST 2012
Química - 2012As fórmulas estruturais de alguns componentes de óleos essenciais, responsáveis pelo aroma de certas ervas e flores, são:
Certas propriedades de cada uma dessas substâncias - FUVEST 2012
Química - 2012Considere os seguintes compostos isoméricos:
CH3CH2CH2CH2OH e CH3CH2OCH2CH3
butanol éter dietílico
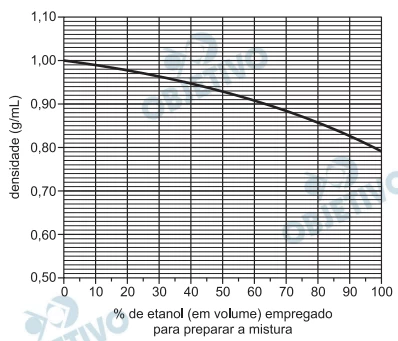
Água e etanol misturam-se completamente, em quaisquer - FUVEST 2012
Química - 2012Água e etanol misturam-se completamente, em quaisquer proporções. Observa-se que o volume final da mistura é menor do que a soma dos volumes de etanol e de água empregados para prepará-la. O gráfico a seguir mostra como a densidade varia em função da porcentagem de etanol (em volume) empregado para preparar a mistura (densidades medidas a 20°C).
Em cadeias carbônicas, dois átomos de carbono podem - FUVEST 2012
Química - 2012Em cadeias carbônicas, dois átomos de carbono podem formar ligação simples (C — C), dupla (C=C) ou tripla (C=-C). Considere que, para uma ligação simples, a distância média de ligação entre os dois átomos de carbono é de 0,154 nm, e a energia média de ligação é de 348 kJ/mol.
O monóxido de nitrogênio (NO) pode ser produzido - FUVEST 2012
Química - 2012O monóxido de nitrogênio (NO) pode ser produzido diretamente a partir de dois gases que são os principais constituintes do ar atmosférico, por meio da reação representada por
N2 (g) + O2 (g) → 2 NO (g) ΔH = + 180 kJ.
O NO pode ser oxidado, formando o dióxido de nitrogênio (NO2), um poluente atmosférico produzido nos motores a explosão:
2 NO (g) + O2 (g) → 2 NO2 (g) ΔH = – 114 kJ.
Tal poluente pode ser decomposto nos gases N2 e O2:
2NO2 (g) → N2(g) + 2O2(g).
Volumes iguais de uma solução de I2 (em solvente - FUVEST 2012
Química - 2012Volumes iguais de uma solução de I2 (em solvente orgânico apropriado) foram colocados em cinco diferentes frascos. Em seguida, a cada um dos frascos foi adicionada uma massa diferente de estanho (Sn), variando entre 0,2 e 1,0 g. Em cada frasco, formou-se uma certa quantidade de SnI4, que foi, então, purificado e pesado. No gráfico abaixo, são apresentados os resultados desse experimento.
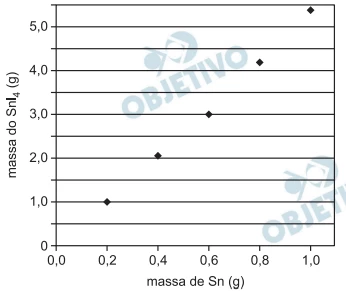
Com base nesses resultados experimentais, é possível afirmar que o valor da relação
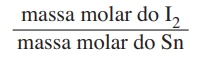
Observa-se que uma solução aquosa saturada de HCl libera - FUVEST 2012
Química - 2012Observa-se que uma solução aquosa saturada de HCl libera uma substância gasosa. Uma estudante de química procurou representar, por meio de uma figura, os tipos de partículas que predominam nas fases aquosa e gasosa desse sistema – sem representar as partículas de água.
A isomerização catalítica de parafinas de cadeia não - FUVEST 2012
Química - 2012A isomerização catalítica de parafinas de cadeia não ramificada, produzindo seus isômeros ramificados, é um processo importante na indústria petroquímica. A uma determinada temperatura e pressão, na presença de um catalisador, o equilíbrio
CH3CH2CH2CH3(g) ←→ (CH3)2CHCH3(g)
n-butano isobutano
Para investigar o fenômeno de oxidação do ferro, fez-se - FUVEST 2012
Química - 2012Para investigar o fenômeno de oxidação do ferro, fez-se o seguinte experimento: No fundo de cada um de dois tubos de ensaio, foi colocada uma amostra de fios de ferro, formando uma espécie de novelo. As duas amostras de ferro tinham a mesma massa. O primeiro tubo foi invertido e mergulhado, até certa altura, em um recipiente contendo água. Com o passar do tempo, observou-se que a água subiu dentro do tubo, atingindo seu nível máximo após vários dias. Nessa situação, mediu-se a diferença (x) entre os níveis da água no tubo e no recipiente. Além disso, observou-se corrosão parcial dos fios de ferro. O segundo tubo foi mergulhado em um recipiente contendo óleo em lugar de água. Nesse caso, observou-se que não houve corrosão visível do ferro e o nível do óleo, dentro e fora do tubo, permaneceu o mesmo.
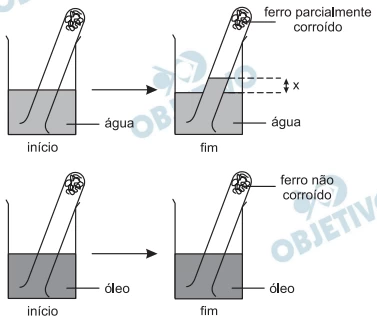
Sobre tal experimento, considere as seguintes afirmações:
I. Com base na variação (x) de altura da coluna de água dentro do primeiro tubo de ensaio, é possível estimar a porcentagem de oxigênio no ar.
II. Se o experimento for repetido com massa maior de fios de ferro, a diferença entre o nível da água no primeiro tubo e no recipiente será maior que x.
III. O segundo tubo foi mergulhado no recipiente com óleo a fim de avaliar a influência da água no processo de corrosão.
Apoie nosso trabalho!
Assine Agora