Disciplina: Química 0 Curtidas
A eletrólise é um processo não espontâneo de grande - Enem 2017
Atualizado em 13/05/2024
A eletrólise é um processo não espontâneo de grande importância para a indústria química. Uma de suas aplicações é a obtenção do gás cloro e do hidróxido de sódio, a partir de uma solução aquosa de cloreto de sódio. Nesse procedimento, utiliza-se uma célula eletroquímica, como ilustrado.
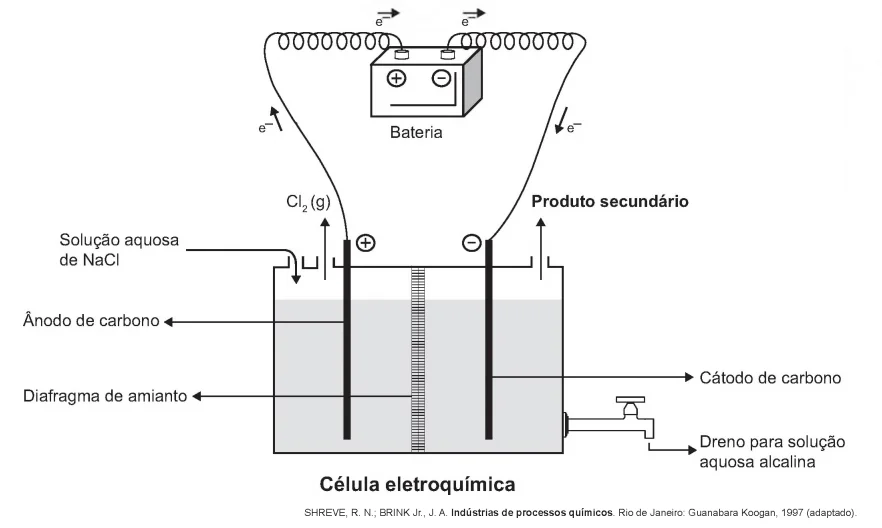
No processo eletrolítico ilustrado, o produto secundário obtido é o
-
vapor de água.
-
oxigênio molecular.
-
hipoclorito de sódio.
-
hidrogênio molecular.
-
cloreto de hidrogênio.
Solução
Alternativa Correta: D) hidrogênio molecular.
O produto secundário é obtido no pólo negativo, que na eletrólise é o catodo, onde ocorre redução do cátion com maior potencial de redução. Como o sódio se mantém na sua forma iônica, formando hidróxido de sódio, deduz-se que o H+ tem maior potencial de redução e se reduz segundo a semi-reação:
2 H+(aq) + 2 é → H2(g),
formando gás hidrogênio como produto secundário.
Créditos da Resolução: Descomplica
Área do Conhecimento: Ciências da Natureza e suas tecnologias
Ano da Prova: 2017
Nível de Dificuldade da Questão: Difícil
Assuntos: Eletrólise, Eletroquímica
Vídeo Sugerido: YouTube