Disciplina: Química 0 Curtidas
Na figura estão representadas as curvas pressão de vapor - VUNESP 2012
Na figura estão representadas as curvas pressão de vapor x temperatura para três solventes puros: benzeno (curva vermelha), água (curva azul) e ácido acético (curva verde).
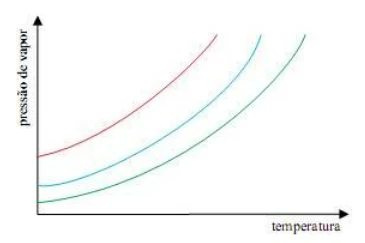
Sobre esses três solventes, é correto afirmar que
-
o ácido acético apresenta a menor temperatura de ebulição a 1 atm.
-
o benzeno apresenta a maior temperatura de ebulição a 1 atm.
-
a água apresenta a maior temperatura de ebulição a 1 atm.
-
na água ocorrem as interações intermoleculares mais intensas.
-
no ácido acético ocorrem as interações intermoleculares mais intensas.
Solução
Alternativa Correta: E) no ácido acético ocorrem as interações intermoleculares mais intensas.
O solvente de menor temperatura de ebulição é o benzeno, pois à mesma temperatura tem maior pressão máxima de vapor. Na água ocorrem interações intermoleculares do tipo ligação de hidrogênio, no ácido acético também ligações de hidrogênio, porém mais intensas, visto que sua temperatura de ebulição é maior devido à sua maior coesão entre as moléculas.
Resolução adaptada de: QConcursos
Institução: VUNESP
Ano da Prova: 2012
Assuntos: Compostos Orgânicos
Vídeo Sugerido: YouTube